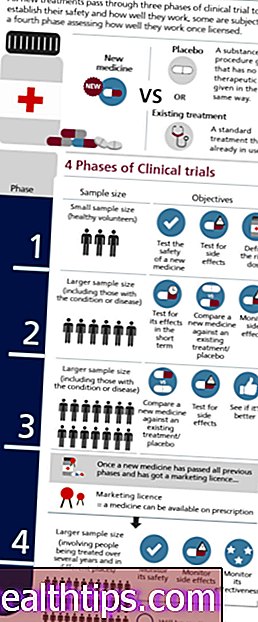
Ogni fase ha uno scopo diverso e aiuta i ricercatori a rispondere a domande diverse.
- Prove di fase I. I ricercatori testano per la prima volta un farmaco o un trattamento in un piccolo gruppo di persone (da 20 a 80). Lo scopo è studiare il farmaco o il trattamento per conoscere la sicurezza e identificare gli effetti collaterali.
- Prove di fase II. Il nuovo farmaco o trattamento viene somministrato a un gruppo più ampio di persone (da 100 a 300) per determinarne l'efficacia e studiarne ulteriormente la sicurezza.
- Studi di fase III. Il nuovo farmaco o trattamento viene somministrato a grandi gruppi di persone (da 1.000 a 3.000) per confermarne l'efficacia, monitorare gli effetti collaterali, confrontarlo con trattamenti standard o simili e raccogliere informazioni che consentiranno di utilizzare in sicurezza il nuovo farmaco o trattamento.
- Prove di fase IV. Dopo che un farmaco è stato approvato dalla FDA e reso disponibile al pubblico, i ricercatori ne monitorano la sicurezza nella popolazione generale, cercando maggiori informazioni sui benefici di un farmaco o di un trattamento e sull'uso ottimale.
Riprodotto con il permesso di NIH Clinical Trials e You. NIH non avalla né consiglia alcun prodotto, servizio o informazione qui descritto o offerto da Healthline. Ultima revisione della pagina il 20 ottobre 2017.